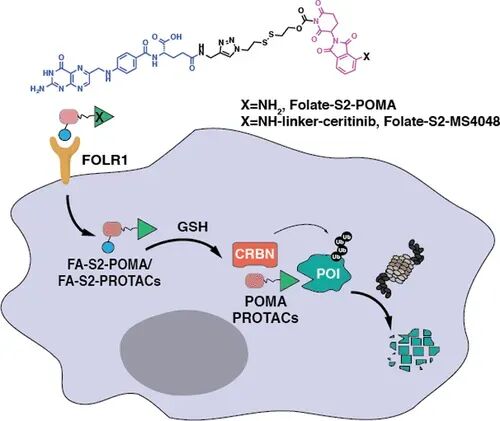
图1 叶酸靶向的SMDC分子
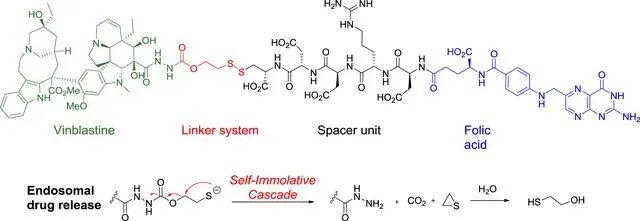
2 Vintafolide分子结构及裂解机制
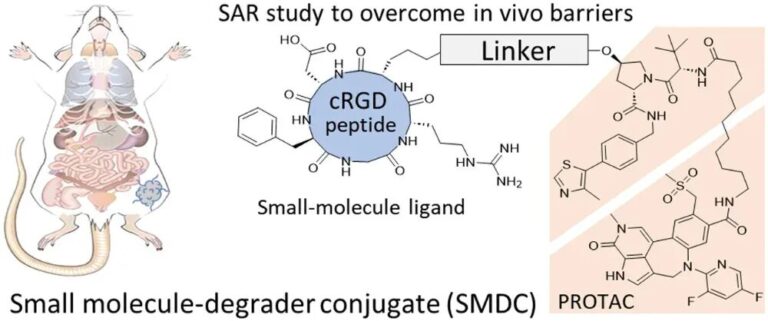
连接子优化过程
表2 处于Ⅲ期开发阶段的蛋白质降解剂
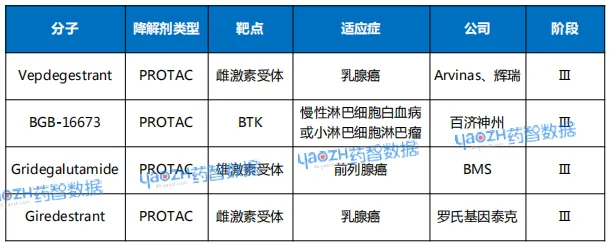
数据来源:公开资料、药智数据
临床开发策略上,大部分TPD候选药物仍处于早期研发阶段,但进入关键III期的资产正在增加。与此同时,对已有初步临床证据的药物进行适应症拓展或联合用药探索,成为价值深挖的重要方向,诺华正在开展其PROTAC药物Luxdegalutamide联合阿比特龙治疗前列腺癌的III期临床试验。
更进一步来说,TPD技术正超越肿瘤学范畴,向更广泛的疾病领域渗透。早期资产已布局在神经退行性疾病、自免及过敏性疾病等。针对帕金森病等相关疾病的ARV-102,以及用于自免病的分子胶MRT-6160,都预示着TPD有潜力成为一种普适性的新药发现平台。
03
TPD赛道的未来王牌
在众多布局TPD的公司中,Kymera、Nurix、Monte Rosa和Beactica凭借其差异化的技术平台和极具潜力的研发管线,构成了该领域的核心力量。
Kymera是TPD领域的先驱之一,专注于利用口服小分子降解剂治疗免疫性疾病,并成功推动首个针对免疫疾病降解剂进入临床。其口服STAT6降解剂KT-621在I期研究中已实现血液和皮肤中STAT6的完全降解,并能降低Th2炎症生物标志物,为特应性皮炎、哮喘等疾病提供新的治疗可能。另一款靶向IRF5的KT-579在临床前狼疮和类风湿性关节炎模型中表现出显著疗效。此外,Kymera通过与赛诺菲合作开发IRAK4降解剂、与吉利德合作开发CDK2降解剂,进一步拓展了其在免疫与肿瘤领域的布局,验证了其平台价值。

图1 Kymera在研管线
图片来源:Kymera官网
Nurix依托其DEL-AI发现平台及广泛的E3连接酶工具箱,在肿瘤和自免领域建立了丰富管线。其DEL-AI平台融合了超过50亿化合物的DNA编码文库、专有E3配体及机器学习模型,能高效探索降解剂化学空间。其领先候选药物Bexobrutinib(NX-5948)为首个获得“-deg”命名的口服、可入脑BTK降解剂,在复发/难治性慢性淋巴细胞白血病等B细胞恶性肿瘤中展现出深度且持久的缓解,且不受基线BTK突变或中枢神经系统受累影响,已准备进入关键试验。此外,双功能降解剂Zelebrudomide(NX-2127)和CBL-B抑制剂NX-1607也显示出在血液瘤和实体瘤中的潜力。Nurix与吉利德、赛诺菲、辉瑞等MNC的合作,进一步体现了其平台技术的跨领域适用性。
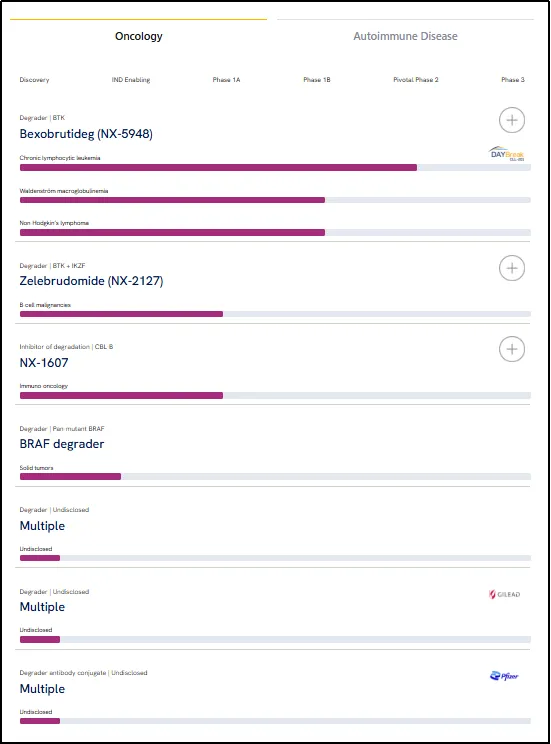
图2 Nurix在肿瘤领域在研管线
图片来源:Nurix官网
Monte Rosa致力于开发“同类唯一”的选择性分子胶降解剂,其QuEEN™发现平台整合了AI引导的化学设计、多样化化合物库、结构生物学与蛋白质组学,以理性设计精准靶向致病蛋白的分子胶。其与诺华合作的VAV1降解剂MRT-6160已进入II期研究;靶向NEK7的MRT-8102处于I期试验,旨在抑制NLRP3炎症小体通路。在肿瘤领域,靶向GSPT1以间接抑制MYC的MRT-2359正在I/II期研究中评估用于去势抵抗性前列腺癌等实体瘤,而针对CCNE1和CDK2的项目已进展至临床前阶段。

图3 Monte Rosa在研管线
图片来源:Monte Rosa官网
Beactica是一家专注于新型作用模式的生物技术公司,以其Eclipsor™平台为核心,开发具有FIC或BIC潜力的变构调节剂与蛋白质降解剂,尤其专注于高难度靶点。目前,其管线中最受关注的是口服LSD1–CoREST降解剂BEA-17,已获FDA授予治疗胶质母细胞瘤的孤儿药资格。该药物旨在逆转肿瘤免疫抑制微环境,临床前研究显示其可通过表观遗传重编程激活抗肿瘤免疫,具有独特治疗定位。另一项目P65-047为双功能TEAD转录因子降解剂,在临床前多种癌症模型中疗效优于同类候选药物。
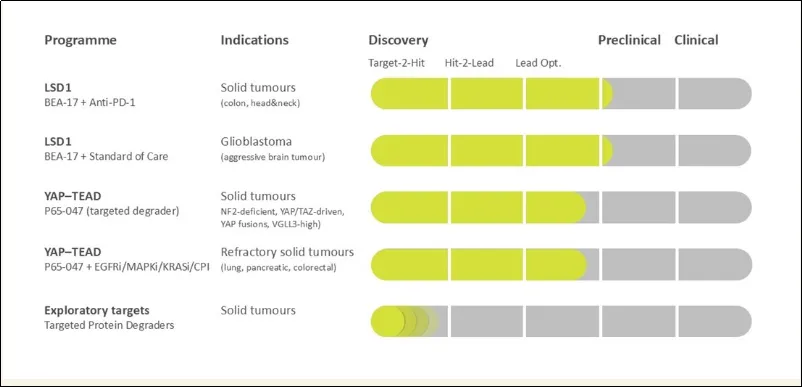
图5 Beactica在研项目
图片来源:Beactica官网
04
结语
随着PROTAC技术逐步实现商业化以及新一代降解技术不断涌现,TPD领域正在从概念探索迈向平台化发展。TPD的浪潮已至,这片曾经被视为“不可成药”的领域,正在开辟出下一代重磅药物的新天地。
参考资料
[1]药智数据
[2]https://ir.arvinas.com/news-releases/news-release-details/arvinas-announces-submission-new-drug-application-us-fda
[3]https://www.clarivate.com.cn/
[4]各企业官网等

