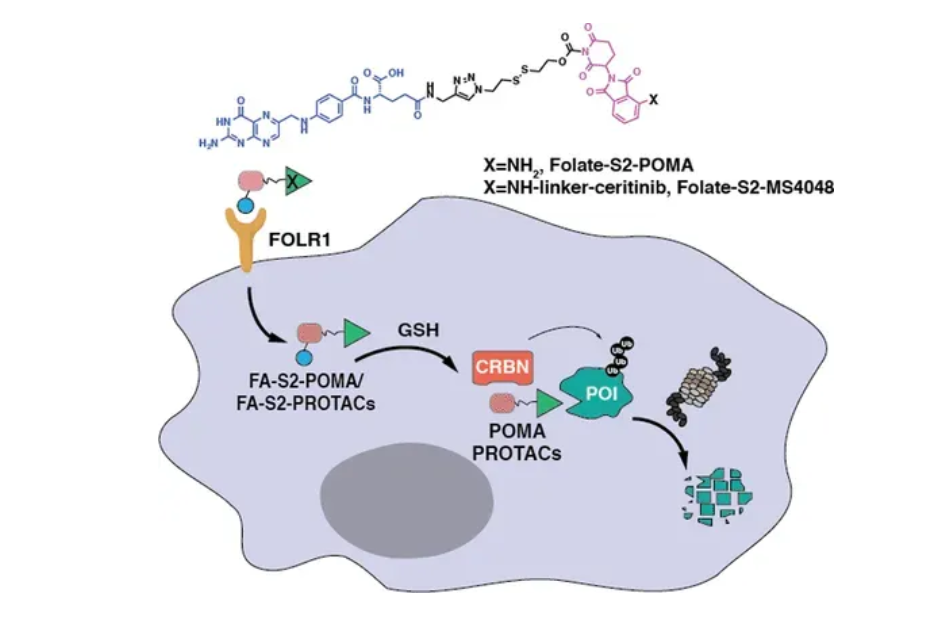
基于叶酸、iRGD 等配体的小分子-降解剂偶联物(SMDC)也已经被开发出来。这类分子在体外能精准降解癌细胞里的目标蛋白,可一到体内,疗效就大打折扣。核心问题就出在连接键不稳定、体内半衰期太短,PROTAC 很难在肿瘤部位有效聚集,效果自然上不去。类似问题在不少小分子偶联药物里都很常见,比如叶酸偶联药 Vintafolide,就是因为这个原因止步 Ⅲ 期临床。
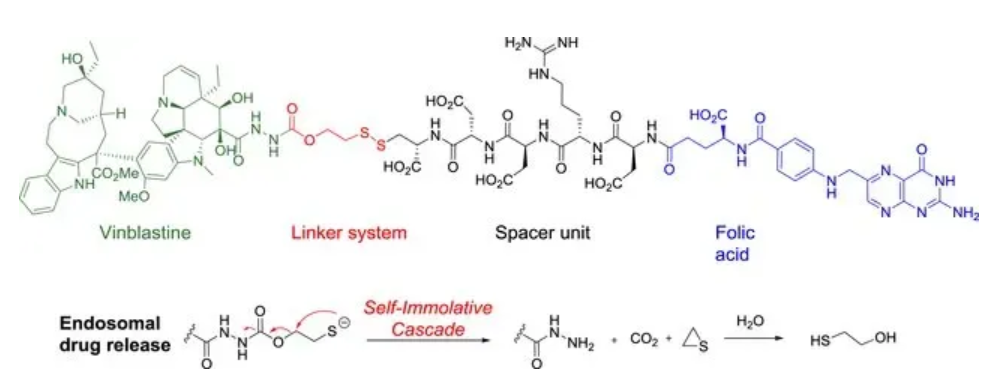
图2 Vintafolide分子结构及裂解机制
连接子作为 SMDC 的核心部分,需要在循环稳定性和肿瘤部位激活释放之间找到精准平衡。虽然 SMDC 的连接子设计和 DACs 有不少相似之处,但受小分子配体本身化学特性影响,还得额外考虑偶联方式、肾脏清除率、稳定性等关键问题,这部分也急需更系统的研究来优化。
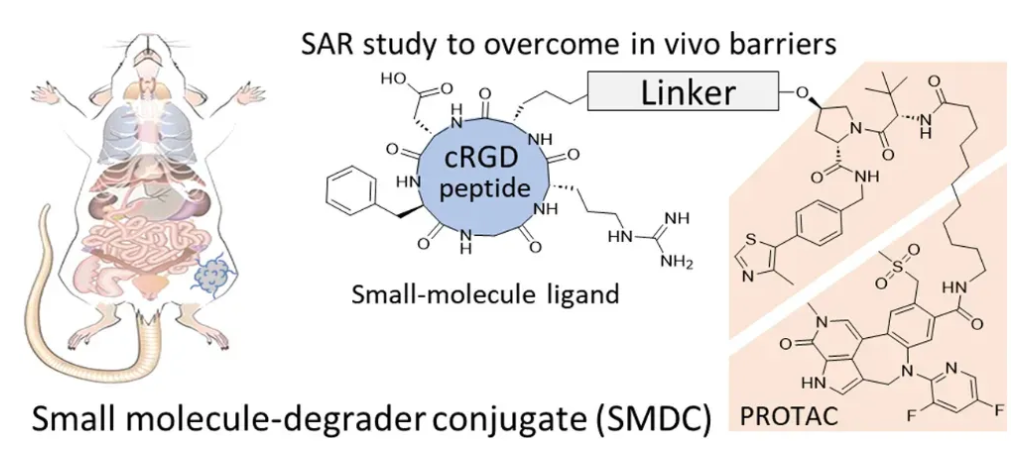
近日,武汉大学的研究团队发表于JMC上的“Small Molecule-Degrader Conjugates: Evaluating theStructure-Activity Relationshipof Linkers to Overcome In VivoBarriers in PROTAC Delivery”探索了SMDC的连接子的结构-活性关系(SAR) 。他们选择cRGD((靶向肿瘤细胞高表达的 αvβ3 整合素)与高活性BRD4 PROTAC GNE-987(DC50=0.03 nM)构建SMDC,,通过四轮优化设计出兼具长循环、高稳定性、肿瘤精准释放的新型连接子,成功克服 PROTAC 体内递送的多重屏障,实现低剂量下的肿瘤生长抑制,为 PROTAC 的精准化、高效化递送提供了全新解决方案。
01
连接子优化过程
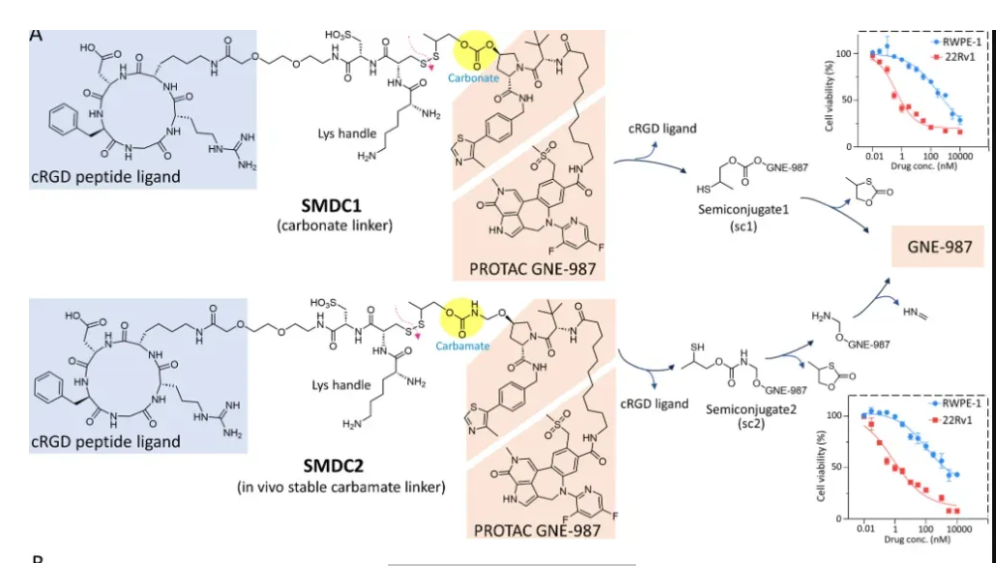
图3 SMDC1及SMDC2的结构
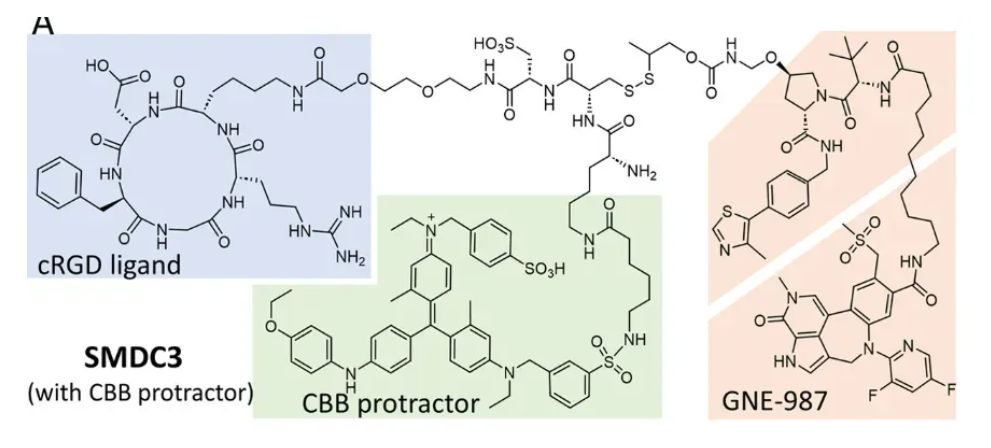
图4 SMDC3结构
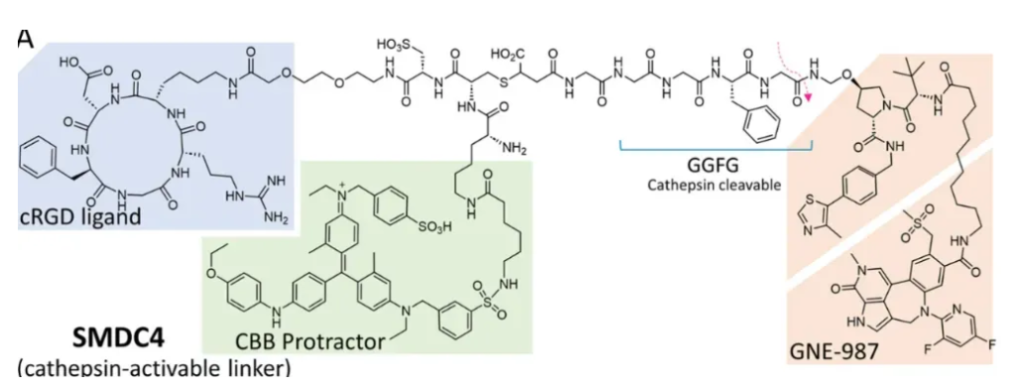
图5 SMDC4的结构
总的来说,这项研究厘清了 SMDC 连接子的核心设计思路:优先选血清稳定的化学键、加白蛋白结合基序拉长体内循环、用肿瘤特异性响应连接子实现精准释放,还巧妙平衡了长循环和肿瘤靶向性,为 PROTAC 靶向递送打造了全新技术范式,开发的连接子模块也很实用,能拓展到多种肿瘤靶点研究中,也为后续 SMDC 的研发和临床转化稳稳打下了基础!

